Человечество с древних времен использует металлы в различных областях. Например, химическая дезинфекция с их использованием практиковалась еще во времена персидской имперской экспансии, около 450 лет до н. э., когда вода хранилась в сосудах из меди или серебра, чтобы сохранить её питьевой. Натрон – сырой нативный натрий карбонат, также использовался для сохранения тел как человека, так и животных. Интересно также отметить, что ряд химических веществ использовался в качестве консервантов древесины. В 1705 году хлорид ртути использовали для консервации древесины и веревок. В практику сульфат меди был введен в 1767 году, а хлорид цинка – в 1815 году [1].
Чем дальше шел прогресс, тем больше обнаруживались новые способы использования металлов в медицине. Так, например, серебро, использовалось для профилактики конъюнктивита у новорожденных и местной терапии ожоговых ран. Также известно об использовании тяжелых металлов в качестве антисептиков или дезинфицирующих средств. К примеру, инактивация бактерий на поверхностях из нержавеющей стали цеолит-керамическими покрытиями, содержащими ионы серебра и цинка. Такие металлы, как серебро, железо и медь, могут быть использованы для дезинфекции воды и медицинских приборов многократного использования, включены в медицинские приборы [2].
Нами было проведено исследование на выявление степени биотоксичности солей металлов по отношению к патогенной микрофлоре методом диффузии в агар (рис. 1).
При анализе полученных данных было установлено, что все сульфаты металлов, кроме MgSO4, подавляют рост P.aeruginosa и S.enterica. Наиболее выраженное проявление подавления роста, вплоть до 1/7 от исходной концентрации в 1 М, наблюдалось у FeSO4 и Cr2(SO4)3. Следует отметить, что AgNO3 и BaNO3 проявляли свою токсичность, лишь по отношению к P.aeruginosa. Бактерии S.enterica оказались устойчивыми к действию данных соединений. Интересным феноменом оказалось то, что сульфаты железа и хрома ингибируют не только рост микроорганизмов, но и влияют на «чувство кворума» бактерий. Это проявлялось в изменении пигментации среды вокруг лунок, что в дальнейшем можно было бы использовать в тестировании различных комбинаций металлов с лекарственными средствами.
Еще одной интересной областью использования металлов в клинической практике, является лечение и профилактика онкологических заболеваний.
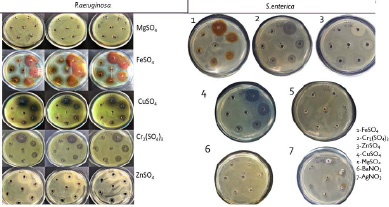
Воздействие солей металлов на рост P.aeruginosa и S.enterica
Механизм антипролиферативного действия металлов может быть различным, в частности, связан с оказанием модулирущего влияния на синтез некоторых онкогенов, направленный на нормализацию неопластической трансформации клеток и ингибирование опухолевого роста или может быть основан на угнетении пролиферации фибробластов, стимулированной фактором их роста [3].
В 1969 году Барнетт Розенберг, Лоретта Ван Кэмп и Томас Кригас опубликовали основополагающую статью, в которой описали антипролиферативную активность очень простого неорганического соединения, сегодня известного как цисплатин [4]. Это открытие, возможно, знаменует собой современное появление темы использования металлов в медицине. Ряд аспектов в истории цисплатина заслуживает внимания [5,6]. Во-первых, это классический пример случайности в науке и тщательных экспериментов с надлежащими контрольными экспериментами, поскольку команда Розенберга фактически изучала совершенно не связанные явления и не намеренно исследовала соединения платины. Во-вторых, первые биологические эксперименты (после того, как были обнаружены морфологические изменения в бактериях) были непосредственно проведены на мышах, а клинические испытания на людях начались еще в 1971 году с одобрения FDA в 1978 году – рекордная скорость по сегодняшним стандартам. Наконец, успех этого, казалось бы, простого неорганического соединения вызвал исследования, которые требовали тесной взаимосвязи биологии и неорганической химии, чтобы прояснить механизм действия Pt-содержащих лекарств и синтезировать новые, потенциально более мощные соединения. В более широком смысле, открытие того, что неорганический комплекс вызвал такой биологический эффект, который Лоретта увидела через линзу своего микроскопа, вдохновило привнести металлоцентрический взгляд в процесс открытия новых лекарств.
Переходные металлы представляют собой группу химических элементов между третьим и двенадцатым столбцами периодической таблицы. Вместе они составляют самую большую ее часть, поскольку включает в себя металлы, такие как медь, золото и титан. Металлы переходной группы также использовались для лечения нескольких заболеваний в течение тысяч лет. Фактически, египтяне были одной из первых известных цивилизаций, которые использовали железо для лечения малярии еще в середине 15-го века до нашей эры.
Переходные металлы обладают большим разнообразием координационных чисел доступными окислительно-восстановительными состояниями в физиологических условиях и широким диапазоном термодинамических свойств и свойств реакционной способности, которые можно успешно регулировать путем выбора подходящих лигандов. Эти характеристики могут быть использованы для разработки новых лекарств с многочисленными преимуществами по сравнению с лекарствами на органической основе, утверждает Лена Руис-Азуара, которая занималась исследованиями, связанными с лечением рака соединениями меди [7].
Исторически сложилось так, что исследования в этой области были сосредоточены на нацеливание на платину и ДНК; однако исследования противоопухолевых препаратов могут быть расширены за счет включения альтернативных соединений металлов с другим механизмом действия, что приводит к заметно разным профилям цитотоксического ответа. Комплексы Купера с выбранными лигандами активно изучаются в качестве агентов для лечения рака. Окислительно-восстановительные свойства как металлов, так и лигандов в комплексах переходных металлов открывают необычные пути для новых механизмов противоопухолевой терапии. Комплексы металлов могут индуцировать окислительно-восстановительный стресс в раковых клетках, включая функциональную активность в качестве фотоактивируемых агентов и катализаторов. Так совсем недавно сообщалось, что комплексы Co и Fe способны проявлять окислительно-опосредованную противоопухолевую активность [8].

